化疗药引发轴突退化,致使NMN堆积
近年来抗癌研究喜报频传,但最常用的还属化疗手段。该文对化疗的严重副作用,外周神经受损进行了机制解读;虽然至今化疗“伤神经”的机制还在完善,但我们已知道NMN“堆积”NAD耗竭是果不是因,而NMNAT功能受损至少是化疗该副作用的原因之一。
癌症的“癌”字真的很形象,数张贪婪的嘴,能把“金山银山”吃个精光,耗竭透支的机体最终因器官衰竭死去。癌症的病因一直未拨云见日,目前较大的声音是年龄:总体而言,癌症发病率与年龄正相关。
01
不可否认我们正处于抗癌的黄金时期,免疫疗法喜报频传,被称为又一次抗癌革命,但是目前最常用的治疗手段还是化疗。
化疗指的是用细胞毒性的化学药物杀死癌细胞,该方法今已有七八十年历史,八十年前的方法现在仍是主流,侧面反映了上世纪攻克癌症的路走得多崎岖。
化疗意味着两个字:痛苦。化疗无差别损害增殖快的细胞,除了癌细胞,头皮、肠道、干细胞都十分活跃,因此也被化疗严重损害,病人出现脱发、腹泻恶心、免疫下降等副作用。
万幸的是,这些副作用大多随着疗程结束,好细胞按部就班,就可慢慢好转愈合,它们属于可逆的化疗副作用。
02
化疗有较大概率诱导外周神经(PNS)损伤,这是大家早就关注却苦手多年的难题。这种神经损伤叫做CIPN(化疗诱导的外周神经损伤,chemotherapy-induced peripheral neuropathy),是进行性、难逆转的。
从轴突退化开始,患者常有感觉异常(麻木、刺痛),随着疗程继续,药物毒性累积,可发展为行动不便或残疾。
常见诱导CIPN的化疗药包括:铂基抗肿瘤药(特别是奥沙利铂和顺铂),长春花生物碱(特别是长春新碱和长春碱),埃坡霉素(伊沙匹隆),紫杉烷类(紫杉醇,多西紫杉醇),蛋白酶体抑制剂(硼替佐米)和免疫调节药物(沙利度胺)。
其中胃肠肿瘤常用药奥沙利铂诱导CIPN概率高达90%。很多患者由于难以承受CIPN,不得不降低了化疗剂量,有甚者被迫中止疗程,权衡严重的CPIN和抗癌疗效,一直是肿瘤治疗让人头疼的事。
从前临床应对CIPN大多采用维生素B族、GSH(还原性谷胱甘肽)、钙镁合剂等,但没什么效果。2018年ASCO大会对CIPN治疗带来了新能量,单唾液神经节苷脂GM1(一种用于帕金森治疗的药物)已被III期临床证实具有预防奥沙利铂CIPN的功效,但在已经发生CIPN且不能停用奥沙利铂的情况下功效如何还在进一步研究中。
CIPN之难难在权衡治疗强度与痛苦,难在理解发病机制和关键分子,而NAD代谢过程在几年前被确认和CIPN有关,这个发现可能为未来临床CNPI的广泛防治带来曙光。
03
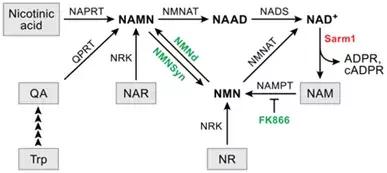
NMNAT,是NAD补救合成途径中的酶,作用为催化烟酰胺单核苷酸(NMN)转化为NAD+,该酶在哺乳动物中有三中同源物,NMNAT1、NMNAT2、NMNAT3,其中NMNAT2在脑中大量表达,常见于胞质;NMNAT1主要表达在细胞核,NMNAT3主要存在于胞质、线粒体。
NMNAT除了在合成NAD、能量代谢中有重要地位,也被发现受压力、损伤诱导,并在损伤后维持神经生存功能有突出效用。
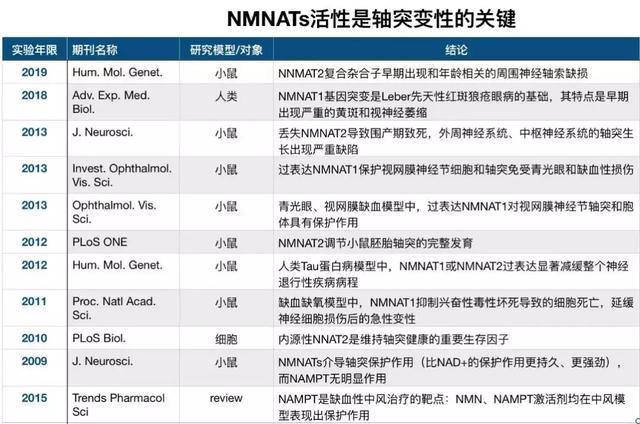
不少动物模型试验证明敲除NMNAT对哺乳动物神经系统造成损伤,过表达NMNAT有助于保护一些疾病模型小鼠的神经系统,目前普遍认为NMNAT是重要的神经保护物质。
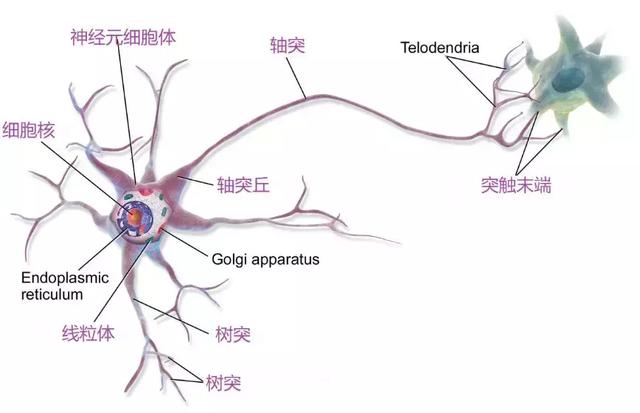
(图:神经元结构)
04
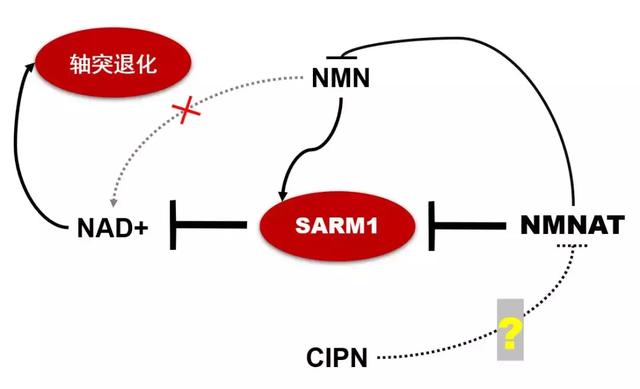
2015年一篇高被引文章曾写道:实验发现病理性轴突退化时局部NMN堆积不下,NAD+耗竭,当使用人为手段抑制NMN合成(使用FK866达成)或将NMN转变为NaMN(使用NMN deamidase达成)时,轴突获得显著的保护,存活时间大大增加。
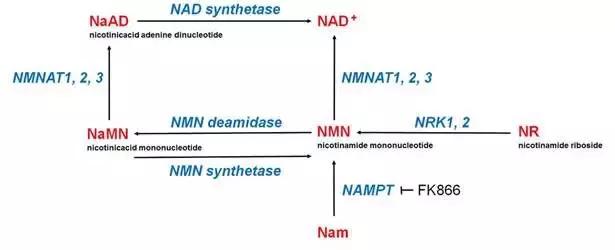
这篇文章开启了NAD/NMN/NMNATs与轴突退化的研究潮,大家致力于研究谁是因谁是果,干预谁将会最有成效。虽然有一段时间大家认为NMN堆积是轴突退化的关键,毕竟“移除”NMN可以显著保护轴突,一份名叫current biology的生物学期刊甚至以《轴突退化:NMN多了有害?》为题刊登过dispatch。但对为什么NMN好像打开开关一样地触发轴突退化却难以回答。2019年,NMN被认为是通过激发SARM1(一种不好的蛋白)生成cADPR(一种Ca2+信使),最后造成细胞死亡。
虽然NMN如何触发轴突破碎才有了一个说法,但SARM1从十年前就与神经细胞的损伤、死亡联系在一起。SARM1可被称作轴突退化启动的刽子手不为过,但究竟是谁在神经疾病或化疗环境下对它发出了“消灭轴突!”的命令,还有待探索。
2016年,科学家使用不同的NAD前体模拟了胞内NMN、NAD高正常低水平的损伤神经模型,发现无论NAD+多或少,无论NMN多或少,均有办法人为保护轴突(且效果还很显著),因此NAD+被耗竭或NMN局部堆积,并不是最重要的轴突退化的原因,它们更像是结伴而来的“果”。

SARM1具有“吃掉”NAD+的能力,我们称能吃掉NAD的这种功能为NADase活性,这种能力平时被NMNAT家族扼住,化疗药毒性导致NMNAT受损,不能有效利用NMN合成NAD,也就是说这条平常流量最大的路,直接给炸毁了。雪上加霜的是神经受损后,会诱导SARM1表达,本来就合成困难,再加消耗增多,NAD+迅速耗竭,导致以轴突退化为先兆的神经变性。
05
2018年,一流期刊PNAS说:倘若NAD代谢中的初始原料能绕过NMN所在的补救途径,通过其他方式合成NAD,轴突将受到良好的形态、功能保护,这种从旁合成稳住了NAD岌岌可危的代谢稳态,大大降低了长春新碱诱导的CIPN对神经元的伤害。
文中的“其他方式”指的是?当然是Preiss-Handler和de novo合成途径。
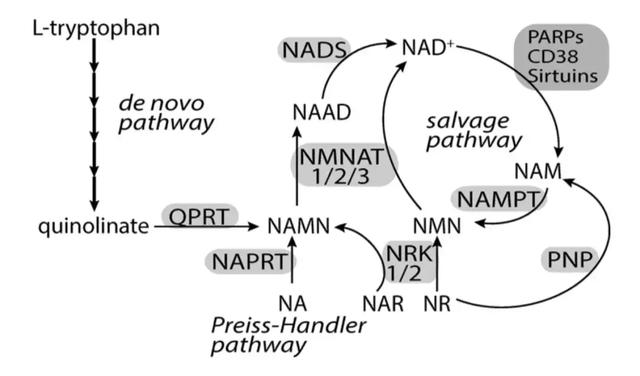
这两种途径分别以L-色氨酸、烟酸或烟酸核苷(NAR)为原料,经繁复步骤合成NAD+。在正常情况下,除了肝脏倾向于色氨酸途径(从头合成途径),消化道、脑、肌肉等组织都喜欢经补救途径(烟酰胺的“旧物回收”途径)合成NAD+,从头途径所供给的NAD和补救途径相比是很少的。
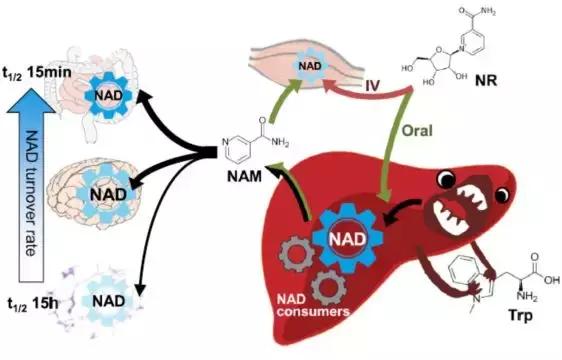
如果说神经节苷脂GM1是事前给神经细胞穿上“盔甲”,那从旁合成NAD就是绕过“地雷”以减少CIPN的伤害,二者皆是有希望的。不过在CIPN情况下,神经细胞的NMNAT即使受损,它们也不会聪明到自己绕过NMN所在补救通路合成NAD,因此人为临床干预化疗患者NAD合成方式是必须的。但介于目前对NAD代谢流、代谢物组织特异性研究才刚起步,虽然这是个实验阶段有很好结果的理论,能否进入临床还需要时间和更多研究考量。
参考文献:
1. Massoll, C., W. Mando, and S.K. Chintala, Excitotoxicity upregulates SARM1 protein expression and promotes Wallerian-like degeneration of retinal ganglion cells and their axons. Invest Ophthalmol Vis Sci, 2013. 54(4): p. 2771-80.
2. Gilley, J., et al., Absence of SARM1 rescues development and survival of NMNAT2-deficient axons. Cell Rep, 2015. 10(12): p. 1974-81.
3. Gerdts, J., et al., SARM1 activation triggers axon degeneration locally via NAD(+) destruction. Science, 2015. 348(6233): p. 453-7.
4. Gerdts, J., et al., Axon Self-Destruction: New Links among SARM1, MAPKs, and NAD+ Metabolism. Neuron, 2016. 89(3): p. 449-60.
5. Sasaki, Y., et al., NMNAT1 inhibits axon degeneration via blockade of SARM1-mediated NAD(+) depletion. Elife, 2016. 5.
6. Essuman, K., et al., The SARM1 Toll/Interleukin-1 Receptor Domain Possesses Intrinsic NAD(+) Cleavage Activity that Promotes Pathological Axonal Degeneration. Neuron, 2017. 93(6): p. 1334-1343 e5.
7. Turkiew, E., et al., Deletion of Sarm1 gene is neuroprotective in two models of peripheral neuropathy. J Peripher Nerv Syst, 2017. 22(3): p. 162-171.
8. Gilley, J., R.R. Ribchester, and M.P. Coleman, Sarm1 Deletion, but Not Wld(S), Confers Lifelong Rescue in a Mouse Model of Severe Axonopathy. Cell Rep, 2017. 21(1): p. 10-16.
9. Geisler, S., et al., Gene therapy targeting SARM1 blocks pathological axon degeneration in mice. J Exp Med, 2019. 216(2): p. 294-303.
10. Zhao, Z.Y., et al., A Cell-Permeant Mimetic of NMN Activates SARM1 to Produce Cyclic ADP-Ribose and Induce Non-apoptotic Cell Death. iScience, 2019. 15: p. 452-466.
11. Cohen, M.S., Axon Degeneration: Too Much NMN Is Actually Bad? Curr Biol, 2017. 27(8): p. R310-R312.
12. Di Stefano, M., et al., A rise in NAD precursor nicotinamide mononucleotide (NMN) after injury promotes axon degeneration. Cell Death Differ, 2015. 22(5): p. 731-42.
13. Liu, H.W., et al., Pharmacological bypass of NAD(+) salvage pathway protects neurons from chemotherapy-induced degeneration. Proc Natl Acad Sci U S A, 2018. 115(42): p. 10654-10659.
14. Liu, L., et al., Quantitative Analysis of NAD Synthesis-Breakdown Fluxes. Cell Metab, 2018. 27(5): p. 1067-1080 e5.

